CDE公開征求《化學仿制藥晶型研究技術指導原則(征求意見稿)》
日期:
2021-09-27
瀏覽次數:
284
2021年9月26日,為進一步明確化學仿制藥晶型研究相關技術要求,CDE起草了《化學仿制藥晶型研究技術指導原則》(征求意見稿),現在CDE網站予以公示,以廣泛聽取各界意見和建議。
CDE原文鏈接:https://www.cde.org.cn/main/news/viewInfoCommon/e90a7d798f1a2a86e6a5798247c9454e
? 1. 概述
? 2.?總體考慮
? ? ?2.1 仿制藥晶型選擇
? ? ?2.3?仿制藥晶型研究思路
? 3.?仿制藥研發中晶型問題的關注點
? ???3.1?晶型與生物利用度/生物等效性
? ? ?3.2?晶型與制劑工藝
? ? ?3.3?晶型穩定性
? ?? 3.4 晶型藥物仿制藥中晶型控制方法的制訂
? 4. 藥物晶型的表征和控制
? ? ?4.1 晶型表征
? ? ?4.2?晶型控制
? 5. 決策樹
? 6. 名詞解釋
??7.?參考文獻
多晶型現象是指同一化學結構分子因存在多種不同的排列形式和分子構象而形成不同晶型的現象。原料藥的不同晶型可具有不同的物理和化學性質,可能對原料藥及制劑的穩定性、制劑的生產工藝、溶出度及生物利用度等產生影響,進而可能影響藥物的安全性、有效性和質量可控性,所以研究原料藥的多晶型現象以及晶型可能對藥物全生命周期各環節產生的影響,是保證藥物質量的核心內容和關鍵環節,對化學仿制藥的研發具有重大意義。本指導原則結合我國仿制藥晶型研究的現狀并參考國外監管機構相關指導原則起草,旨在明確仿制藥晶型研究過程中的關注點,涉及的晶型包括無水物、水合物、溶劑合物和無定型等。
本指導原則僅代表藥品監管部門目前對于該問題的觀點和認知。隨著科學和技術的進展,本指導原則中的相關內容將不斷完善與更新。申請人應基于風險評估的理念,在全面理解參比制劑目標質量概況的基礎上,選擇適宜的晶型進行處方工藝開發。化學仿制藥晶型研究主要包括兩方面內容:一是原料藥多晶型的種類,重點晶型的制備、表征及理化性質研究;二是原料藥多晶型對制劑工藝和療效等可能產生的影響,根據研究結果選擇適宜晶型。
1. 仿制藥晶型選擇
申請人應對原料藥的多晶型現象有足夠的認識。可以通過科學文獻、專利以及其他相關的參考資料,或通過晶型篩選試驗獲得相關數據。晶型篩選應關注在原料藥和制劑制備和貯存過程中可能會生成或轉化的晶型。對于仿制藥,通常情況下應選擇與參比制劑一致的晶型,若有足夠的試驗數據證實其他晶型制備的仿制藥與參比制劑生物等效且具有合適的穩定性,也可選擇與參比制劑不同的晶型。無論選擇何種晶型,均應對所選擇晶型進行充分的理化性質和穩定性研究。
2. 仿制藥晶型研究思路
對于仿制固體制劑、半固體制劑和混懸劑,應主要考慮晶型對原料藥及制劑工藝和穩定性的影響,以及對制劑溶出和生物利用度/生物等效性的影響,在充分研究晶型對其影響的基礎上,確定是否有必要對藥物的晶型進行控制。對于液體制劑(如口服液、注射液等),建議關注原料藥的不同晶型對制劑工藝過程可能產生的影響。
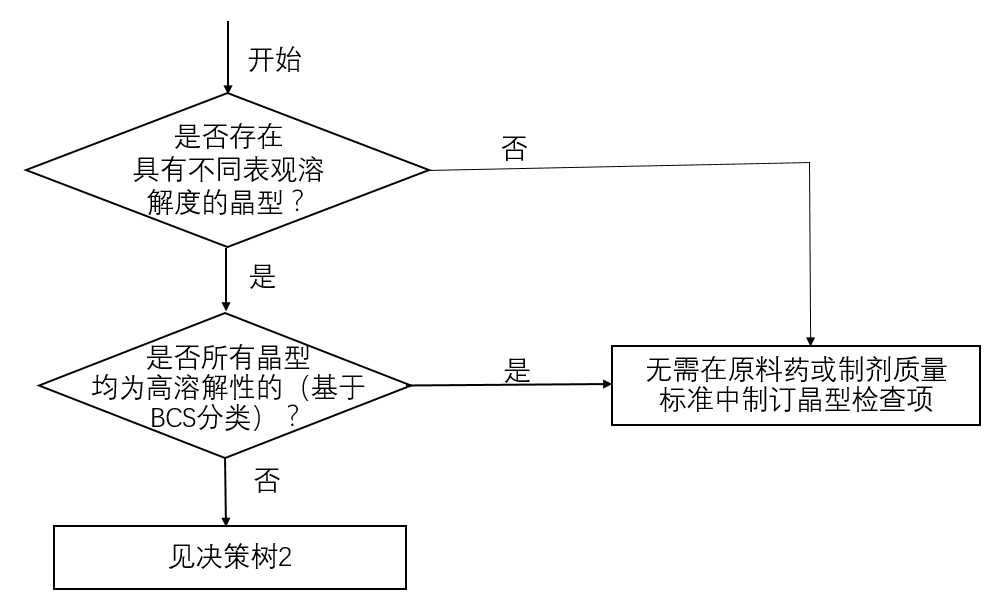
由于原料藥不同晶型的內部分子排列或分子構象不同,所以可能存在溶解度和溶解速率的差異。當原料藥不同晶型的表觀溶解度存在差異時,建議申請人關注這種差異是否會影響制劑生物利用度/生物等效性。原料藥不同晶型的表觀溶解度差異是否會影響制劑生物利用度/生物等效性,取決于影響藥物吸收速度和程度的各種生理學因素,包括胃腸道蠕動、藥物的溶出、藥物的滲透性等。此時,生物藥劑學分類(BCS)可科學地評價多晶型現象對制劑生物利用度/生物等效性影響程度,使用BCS分類進行評估時,應自證擬開發品種的BCS分類。對于體內吸收僅受溶出速度限制的高滲透性藥物,若不同晶型之間表觀溶解度差異較大,就很可能影響生物利用度/生物等效性。而對于吸收僅受腸道滲透性限制的低滲透性、高溶解性藥物,各晶型之間的表觀溶解度的差異對生物利用 度/生物等效性的影響相對較小。對于高溶解性藥物,當各晶型的表觀溶解度均足夠大,藥物的溶出速度快于胃排空速度時,各晶型之間的表觀溶解度的差異對生物利用度/生物等效性的影響不明顯。在證明仿制藥與參比制劑體內生物等效后,溶出度檢查可用于評價仿制藥的批間一致性。當晶型轉變可能影響制劑的生物利用度或生物等效性時,可通過溶出度檢查作為監控方法,但應提供研究資料論證所用溶出方法能反映上述變化。原料藥的不同晶型可呈現不同的物理和機械性質,包括吸濕性、顆粒形狀、密度、流動性和可壓性等,進而可影響原料藥的純化和/或制劑的生產。鑒于原料藥多晶型可影響制劑工藝的穩健性,故建議申請人密切關注原料藥的多晶型。多晶型對制劑生產過程的影響還與制劑處方和工藝有關。例如,對于粉末直壓的工藝,尤其是當原料藥在處方中所占的比例較大時,原料藥的固態特征是藥物制劑生產的關鍵影響因素;而對于濕法制粒工藝,原料藥的固態特征通常被制粒過程所改變或掩蓋,其固態特征對生產的影響可能就比較小。關于原料藥多晶型對制劑工藝的影響,需要考慮的關鍵問題是確保能夠持續穩定地生產出符合過程控制和放行標準的制劑。原料藥經干燥、粉碎、制粒和壓片等制劑工藝步驟,在溫度和濕度等環境因素的作用下,均可能出現轉晶現象,其晶型轉變的程度往往取決于不同晶型的相對穩定性、相轉變能壘,以及外加應力。應對工藝過程中晶型轉變情況進行充分的研究。在藥物開發過程中,為了降低轉晶的可能性,以及得到更好的化學穩定性,通常選擇熱力學最穩定的晶型。在某些情況下(如基于提高難溶性藥物生物利用度等考慮)如果選擇亞穩態晶型或無定型作為開發晶型,應證明所選擇晶型在生產和貯存過程中具有足夠的物理和化學穩定性,特別關注藥物晶型的穩定性,并采取適當的措施(如適當的處方、生產工藝、包裝等)避免在貯存期間亞穩態晶型向穩定型晶型轉變。決策樹1-3為仿制藥申請人提供了策略過程,該過程用以評估多晶型對晶型藥物仿制藥的重要性,以及制訂晶型控制方法的各種方式。雖然決策樹采納的理論框架主要是基于多晶型影響制劑生物等效性/生物利用度的潛在因素而建構,但建議申請人仍要考慮多晶型對制劑工藝穩健性產生的影響,以及對制劑穩定性產生的影響。決策樹1為原料藥和/或制劑標準中制訂晶型檢查項的建議。如果原料藥所有晶型表觀溶解度沒有差異或者均為高溶解性,則原料藥的不同晶型對生物利用度/生物等效性產生顯著影響的可能性較小,因此通常情況下無需在原料藥和/或制劑中制訂晶型檢查項。
按照BCS分類系統對藥物的溶解性進行區分,當原料藥的至少一種晶型屬于低溶解性時,可參考決策樹2制訂該原料藥晶型檢查項。若中國藥典中收載了晶型檢查項,且該項適用于目標晶型的控制,可在原料藥質量標準中采用與藥典相同的晶型檢查項。若中國藥典沒有收載晶型檢查項,或該項不適用于目標晶型的控制,申請人應參考相關文獻(如,其他國家藥典等)并在充分研究的基礎上制訂新的晶型檢查項。
可參考決策樹3選擇制劑中晶型的控制策略。通常,如選擇的晶型是熱力學最穩定的晶型,或者選擇與參比制劑使用相同的晶型,通常情況下無需在制劑質量標準中制訂晶型檢查項,但如果選擇的是亞穩態晶型,由于亞穩態晶型可能在制劑工藝和貯存過程中發生晶型轉變,需要進行相關研究并依據研究情況決定是否在制劑質量標準中制訂晶型檢查項。對于難溶性藥物,如果晶型變化對生物利用度/生物等效性的影響可通過制劑的性能檢測(如,溶出度)進行控制時,可通過溶出度等性能檢測項替代晶型控制。如果需要對晶型 進行控制,且難以建立制劑其他質控指標與晶型之間關系時,應在制劑質量標準中制訂反映晶型變化的其他檢測項(如,固態表征等)。常用的晶型表征方法包括:單晶X射線衍射法(SXRD)、粉末X射線衍射法(PXRD)、紅外光譜法(IR)、拉曼光譜法(Raman)、差示掃描量熱法(DSC)、熱重法(TG)、毛細管熔點法(MP)、光學顯微法(LM)、偏光顯微法(PM)、固體核磁共振波譜法(ssNMR)等。其中,單晶X射線衍射法和粉末X射線衍射法是目前公認的最可靠方法。熱分析方法(如,差示掃描量熱法、熱臺顯微鏡法等)和光譜法等(如,紅外光譜法、拉曼光譜、固體核磁共振波譜法等)均可進一步支持不同晶型的確證。
鑒于上述所提及的表征方法多數僅能反映不同晶型某一方面的物理性質,因此,申請人應結合申報品種和擬采用晶型的特點等選擇適宜的方法對晶型進行表征。
可參照《中國藥典》相關通則對晶型進行定性和/或定量分析。其他國際公認用于物相分析的方法也可對晶型進行定性或定量分析,確保原料藥或制劑中有效晶型的含量。常用的定量方法包括:粉末X射線衍射法(PXRD)、紅外光譜法(IR)、差示掃描量熱法(DSC)、拉曼光譜法(Raman)、固體核磁共振波譜法(ssNMR)等。決策樹1 制訂晶型檢查項的必要性

決策樹3 制劑晶型檢查項的制訂
多晶型現象(同質異晶現象):描述固體化學藥物物質狀態,可由一組參量(晶胞參數、分子對稱性、分析排列規律、分子作用力、分子構象、結晶水或結晶溶劑等)組成,當這些參量中的一種或幾種發生變化,而使其存在有兩種或兩種以上不同的固體物質狀態。晶態:指分子在晶格中具有周期性、對稱性的排列規律。
晶型藥物:指藥效成分以特定晶型狀態存在的固體藥物,尤其是固體化學藥物。
無定型:指分子的排列沒有周期性規律。
無水物:指不含結晶水或結晶溶劑的晶態物質。
溶劑合物:指含有化學計量或非化學計量溶劑的晶型物質。
水合物:如果溶劑合物的溶劑為水,該溶劑合物通常被稱為水合物。
表觀溶解度:物質在表觀平衡(過飽和)狀態下的濃度。表觀溶解度不同于真正的熱力學溶解度,真正的熱力學溶解度是在無限平衡時達到的。
轉晶現象:化合物晶型物質狀態因環境條件變化(如:溫度、濕度、光照、壓力等)而從某種晶型物質狀態轉變為另外一種晶型物質狀態。
熱力學最穩定晶型:具有多晶型的化合物,在給定溫度和壓力下,吉布斯自由能最低的形式。
1.?國家藥品監督管理局《藥品注冊管理辦法》(2020年 1月22日國家市場監督管理總局令第27號)2.?國家食品藥品監督管理總局《化學藥品注冊分類改革 工作方案》(2016年3月)3.?國家食品藥品監督管理總局藥品審評中心《化學藥物 原料藥制備和結構確證研究的技術指導原則》(2005年3月)4.?國家食品藥品監督管理總局藥品審評中心《化學藥物 制劑研究基本技術指導原則》(2005年3月)5.?國家食品藥品監督管理總局藥品審評中心《已有國家 標準化學藥品研究技術指導原則》2007年6.?國家食品藥品監督管理總局《化學藥物(原料藥和制 劑)穩定性研究技術指導原則》(2015年第3號)7. 國家食品藥品監督管理總局:總局關于發布化學藥品新注冊分類申報資料要求(試行)的通告(2016 年第80 號)8. 國家食品藥品監督管理總局:總局關于發布化學藥品 仿制藥口服固體制劑質量和療效一致性評價申報資料要求(試行)的通告(2016年第120號)9.《中國藥典》2020年版四部通則,9015藥品晶型研究及晶型質量控制指導原則10. ICH Q3A: Impurities in New Drug Substances. 200611. ICH Q6A: Specifications Test Procedures and AcceptanceCriteria for New Drug Substances and New Drug Products Chemical Substances.199912. Food and Drug Administration. Guidance for Industry. ANDAs:Pharmaceutical Solid Polymorphism. July 200713. USP General Chapters<1236>:SOLUBILITYMEASUREMENTS14. USP General Notices and Requirements15. EUROPEAN PHRMACOPOEIA 10.0: 5.9. POLYMORPHISM16. JP17 XVII General Tests2.58:X-Ray Powder Diffraction Method17. WHO Technical Report Series 970,WHO Expert Committee on Specifications for Pharmaceutical Preparations,Forty-sixth report.18. WHO POLYMORPHISM Draft chapter for The International Pharmacopoeia. December 2018.